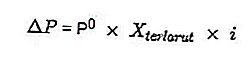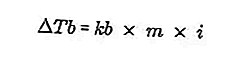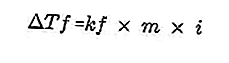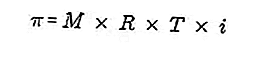Intenta prestar atención a lo que nos rodea relacionado con la química. El más fácil es el aire que respiramos, que contiene una mezcla de oxígeno, nitrógeno y otros gases. Los condimentos, colorantes alimentarios y conservantes alimentarios también son otros ejemplos de sustancias químicas que nos rodean. La química es una rama de las ciencias naturales que estudiarás en la escuela que estudia diversos materiales, un ejemplo es la estructura de la materia, propiedades de la materia, forma material, cambios en la materia, clasificación de la materia, composición de la materia y energía que acompañan a estos cambios. No solo las matemáticas y la física, la química también tiene varios tipos de fórmulas, ya sabes. Hay muchas fórmulas químicas de las que aprenderá, desde propiedades coligativas hasta reacciones redox.
En esta ocasión aprenderemos diversas fórmulas químicas y también ejemplos de sus problemas que te ayudarán a comprender los conceptos de fórmulas químicas.
Fórmulas químicas y problemas de ejemplo
La presencia de fórmulas en química sirve para ayudar a los investigadores a encontrar diversos tipos de resultados experimentales que se van a realizar. Para poder dominar bien esta ciencia, debe conocer algunas fórmulas químicas que encontrará a menudo al estudiar química.
Fórmula para las propiedades coligativas de las soluciones
La naturaleza coligativa de una solución es una característica de una solución que no depende de un tipo de sustancia soluble, sino que solo depende de la concentración de las partículas de la solución. Entonces, la naturaleza coligativa de la solución consta de dos tipos de propiedades, a saber, la naturaleza coligativa de la solución electrolítica y la naturaleza coligativa de la solución no electrolítica.
- Propiedades coligativas de soluciones no electrolíticas
Aunque la naturaleza coligativa implica una solución, la naturaleza coligativa no depende de la interacción de las moléculas de soluto y soluto, sino de la cantidad de soluto disuelto en una solución. Las propiedades coligativas consisten en una disminución de la presión de vapor, aumento del punto de ebullición, disminución del punto de congelación y presión osmótica. Cada uno requiere una fórmula química para obtener el resultado.
- Ecuación de caída de presión de vapor

Fuente: formula.co.id
- Ecuación de aumento del punto de ebullición
El punto de ebullición de un líquido es la temperatura fija a la que hierve. A esta temperatura, la presión de vapor del líquido tiene una ecuación en la presión del aire a su alrededor y es causada por la evaporación de todas las partes del líquido. El punto de ebullición de un líquido se puede medir con una presión de 1 atmósfera.
La diferencia en el punto de ebullición de una solución y el punto de ebullición de un disolvente puro se llama aumento del punto de ebullición, la ecuación para el aumento del punto de ebullición es:

Fuente: formula.co.id
- Ecuación de caída del punto de congelación
Un soluto presente en solución hará que el punto de congelación de la solución sea más pequeño que el punto de congelación del solvente. Ecuación de reducción del punto de congelación:

Fuente: formula.co.id
- Presión osmótica
La presión osmótica es una fuerza necesaria para equilibrar la presión del disolvente desde la membrana semipermiable a través de la solución.
Una membrana semipermeable es una membrana a través de la cual pueden pasar las moléculas de disolvente, pero los solutos no pueden. Según Van't Hoff, a la presión osmótica, la solución se formula de la siguiente manera:

Fuente: formula.co.id
- Propiedades coligativas de las soluciones de electrolitos
En la concentración, las propiedades coligativas de la misma solución electrolítica tienen un valor mayor cuando la comparamos con las propiedades coligativas de la solución no electrolítica. Porque la gran cantidad de partículas de soluto resulta de la reacción de ionización de la solución de electrolito que se ha formulado en el factor Van't Hoff.
El cálculo de las propiedades coligativas de las soluciones de electrolitos siempre se multiplicará por el factor de Van't Hoff de la siguiente manera:

Fuente: formula.co.id
Algunas de las fórmulas para las propiedades coligativas de otras soluciones de electrolitos son:
- Caída de la presión de vapor
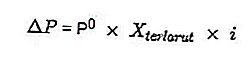
Fuente: formula.co.id
- Aumento del punto de ebullición
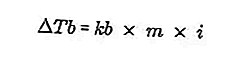
Fuente: formula.co.id
- Caída del punto de congelación
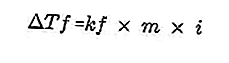
Fuente: formula.co.id
- Presión osmótica
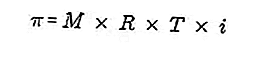
Fuente: formula.co.id
Fórmulas de molaridad, molalidad y fracción molar
Molaridad (M)
La molaridad es el número de moles de una sustancia disueltos en 1 litro de solución.

Fuente: formula.co.id
M = molaridad
Mr = masa molar del soluto (g / mol)
V = volumen de solución
Molalidad (m)
La molalidad es el número de moles de la sustancia disueltos en 1 kg de disolvente. La fórmula química es la siguiente.

Fuente: formula.co.id
m = molalidad (mol / kg)
Mr = masa molar del soluto (g / mol)
masa = masa del soluto (g)
P = masa de disolvente (g)
Fracción mol
La fracción molar es una unidad de concentración en la que todos los componentes de la solución se calculan en función de los moles.

Fuente: formula.co.id
xi = número de moles
i, j, xj = fracción molar
Ejemplos de problemas de fórmulas químicas
1. Si la presión osmótica de 500 ml de solución de fructosa, C6H12O6 de 32 ° C es 2 atm, ¿la masa de fructosa disuelta es?
Solución:

2. En la fracción molar de solución de urea en agua 0,2. La presión de vapor saturado de agua pura con una temperatura de 20 ° C es de 17,5 mmHg. Entonces, a la solución saturada, la presión de vapor a la siguiente temperatura es?
X urea + X agua = 1
0.2 + X agua = 1
X agua = 0,8
Solución P = X agua x P agua
P de la solución = 0,8 x 17,5 mmHg
P de solución = 14 mmHg
Estas son algunas fórmulas químicas que puede aprender para que le resulte más fácil responder a varios tipos de preguntas sobre química. Si cree que estas fórmulas no son suficientes, puede probar el producto PROBLEM, una solución de práctica en línea ponderada y completa para la clase inteligente, como Trigonometría, Límite, Logaritmo y muchos más. Desde los niveles de primaria, secundaria hasta bachillerato con diversas materias como matemáticas, física, química y otras. Aquí puede aprender varios tipos de fórmulas completas con ejemplos del problema.
¡Vamos, qué estás esperando! Probemos ahora mismo los ejercicios PROBLEM en Smart Class.